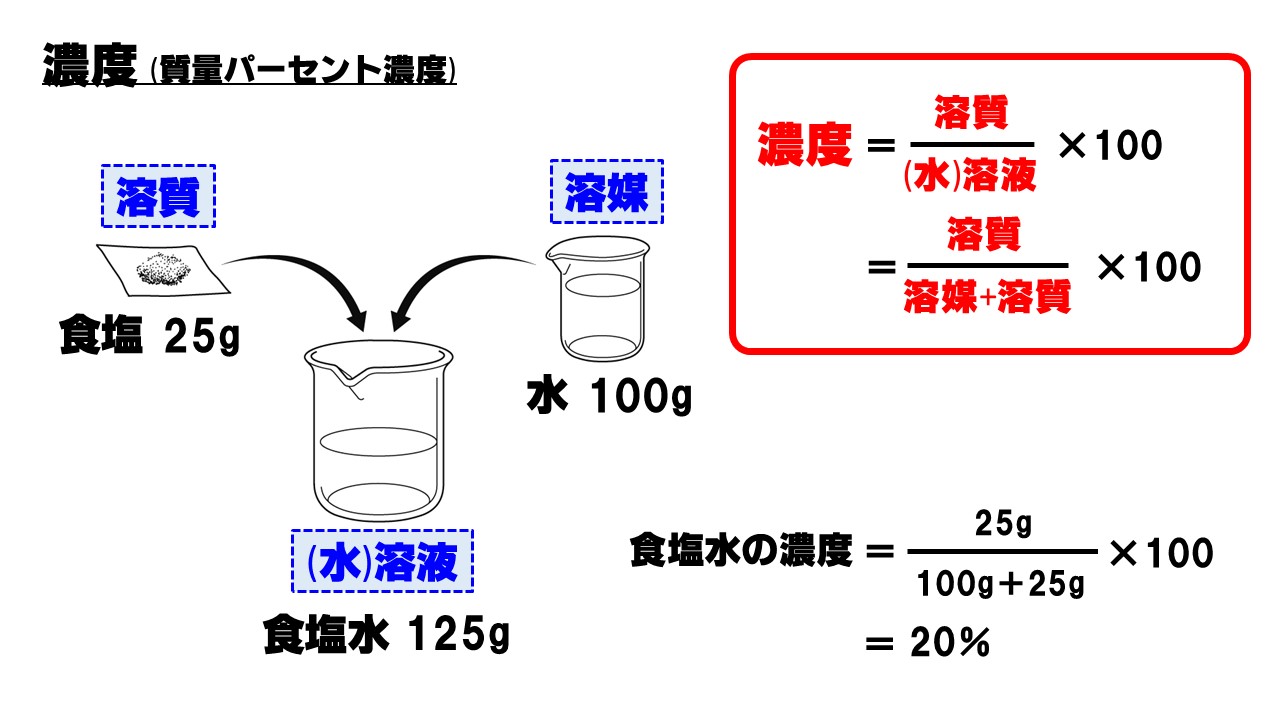
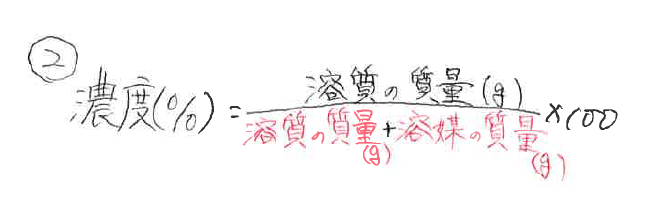
「質量パーセント濃度」 溶液の質量に対する溶質の質量の割合を 百分率で示したもの 求め方 質量パーセント濃度(%) 溶質の質量(g) = × 100 溶液の質量(g) 溶質の質量(g) = × 100 質量パーセント濃度の求め方がわかったところで、練習問題をやってみましょう。 問題1 gの食塩を水に溶かして400gにしました。この食塩水の質量パーセント濃度を求めましょう。 解答 質量パーセント濃度(%)= 溶質の質量(g)÷ 溶液(溶質溶媒)の質量(g)× 100 なので 質量パーセントと体積パーセントの区別がつきません。 両方とも無次元ということと、質量パーセントの求め方 濃度 (mol/L)*分子量 (g/mol)*密度の逆数 (cm3/g)*単位変更 (dm3/cm3)*100= wt% です。 解る方いらっしゃいましたら、両者の違いと、体積
化学講座 第12回 濃度と密度 私立 国公立大学医学部に入ろう ドットコム
質量 パーセント 濃度 求め方
質量 パーセント 濃度 求め方- モル濃度のモルは物質量の単位のことです。求め方は以下の通りです。 質量パーセント濃度と式の形は似ていますが、 大きな違いはやはり100倍しないことですね。 というのも、 単位が%ではないので100倍する必要が無いのです。動画一覧や問題のプリントアウトはこちらをご利用ください。ホームページ → http//19chtv/ Twitter→ https//twittercom/haichi_toaru



50g15 0g Descubre Como Resolverlo En Qanda
②質量パーセント濃度の求め方 白枝先生 では、質量パーセント濃度はどうやって求めるのでしょうか? 先ほども言いましたが質量パーセント濃度は「 ある溶液中に溶けている溶質の割合 」です。 つまり、溶質の質量が溶液の質量のどれだけを示すのかを表すものになります。 それを踏まえ溶質の質量÷水溶液の質量×10 質量パーセント濃度 をどのように求めるかというと、次の式に当てはめます。 質量パーセント濃度〔%〕= (溶質の質量〔g〕/溶液の質量〔g〕)×10 方程式を使う解き方 今回求めたいのは 「加える水の質量」 です。だから 「加える水の質量」 を xg として計算を進めます。 そう考えると、 水を加えた後の塩酸の質量が (450x) g;
質量パーセント濃度 をどのように求めるかというと、次の式に当てはめます。 質量パーセント濃度〔%〕= (溶質の質量〔g〕/溶液の質量〔g〕)×100PH値の求め方|基礎講座|技術情報・便利ツール|株式会社タクミナ 基礎講座|pH中和処理制御技術 23 pHとは? pH値の求め方 少し数学的に表現するとpHは、つぎのように定義されます。 pH =-logH logとは、対数(ロガリズム)のことで、x=10 n のこんにちは!この記事を書いてるKenだよ。握りたいね。 中1の理科では、 質量パーセント濃度の求め方の公式 を勉強したよね?? 「公式は覚えられそうだけど、テスト
質量パーセント濃度の求め方 *一般的な濃度の計算式です。 質量パーセント濃度 % = 溶質の量 g ÷ 溶液(溶媒+溶質)の量 g × 100 *パーセント(百分率)濃度なので、100倍にします。 つまり、100g(溶液の質量) 中に含まれている溶質の量の割合を 求めることにより濃度がわかります。 *質量 質量パーセント濃度(%)=溶質の質量÷溶液の質量×10� エタノールが溶液全体の何wt%であるかを求めるので、 (g)/500 (g)×100= 4 (wt% 濃硫酸1Lの質量は、 1L = 1000cm³ 1000cm³ × 18g/cm³ = 1800g 質量パーセント濃度が98%なので、溶けているH₂SO₄の質量は�質量パーセント濃度が 22% 、密度が 12g/mL の水酸化ナトリウム水溶液があります。 この水溶液の モル濃度 を求めていきましょう。 さて、どのようにしてモル濃度を求めるか、イメージできますか?




4 6 溶液の濃度 おのれー Note
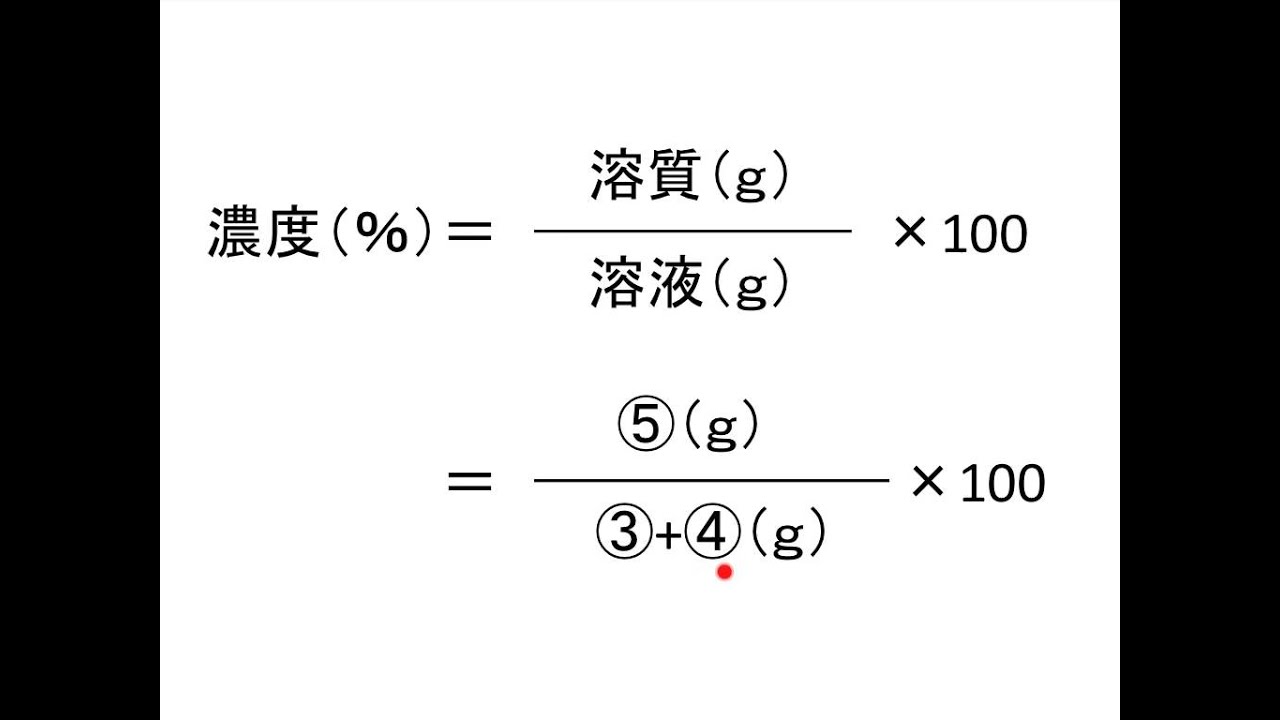



濃度の求め方 絵で覚えよう Youtube
水溶液の濃度(質量パーセント濃度):公式と求め方 水溶液の濃さは溶質の質量を水溶液の質量で割って100をかけて求めます。 溶質の質量÷水溶液の質量×100 この値を質量パーセント濃度ともいいます。単に濃さという場合は、この質量パーセント濃度を ・mol濃度⇄質量パーセント濃度⇄質量モル濃度の相互変換や、 ・密度との関係を理解して、 "自由自在にあやつれる"ようにするために大切な、「単位」の考え方まで紹介しています。 具体例(解説・練習用問題付き) 目次(タップした所へ飛びます) 濃度は単位に注目せよ!~3種類を攻質量パーセント濃度の単位は%(パーセント)。公式は以下のようになります。 公式は以下のようになります。 質量パーセント濃度 % =(溶質 g / 溶液 g)×100




これで理科マスター 質量パーセント濃度を計算する5つの問題 Qikeru 学びを楽しくわかりやすく
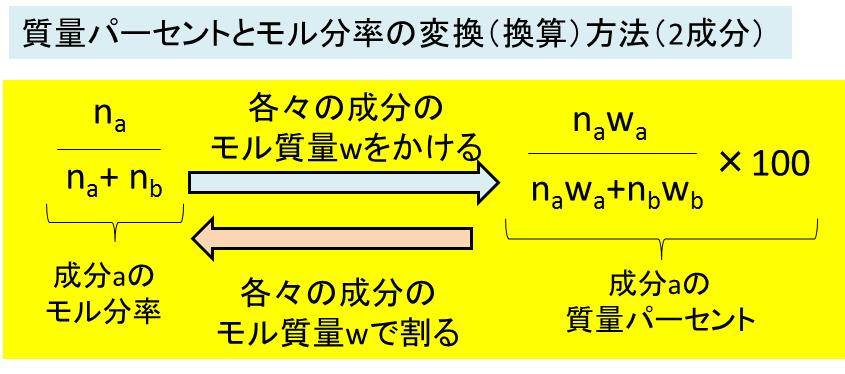



質量パーセントとモル分率の変換 換算 方法 計算
パーセントの意味は下記が参考になります。 百分率とは?1分でわかる意味、割合との違い、少数、分数との関係 スポンサーリンク wt%の計算 下図をみてください。水100gと砂糖10gがあります。水の中に砂糖を入れました。砂糖の濃度を計算しwt%で表しましょう。 前述した式を思い出して質量パーセント濃度 公式 覚え方 質量パーセント濃度を計算する問題を出してほしい! wt%は「ウェイトパーセント」と読みます。 ウェイトパーセントは、 溶質(溶かしている物質)の重さ $\div$ 全体の重さ で計算できます。 例えば、5グラムの食塩と95グラムの水を混ぜて、100グラムの食塩水を作ったときのwt%は、 $5\div 100=005$ つまり 5wt% になります。 参考:食塩水の濃度を計算
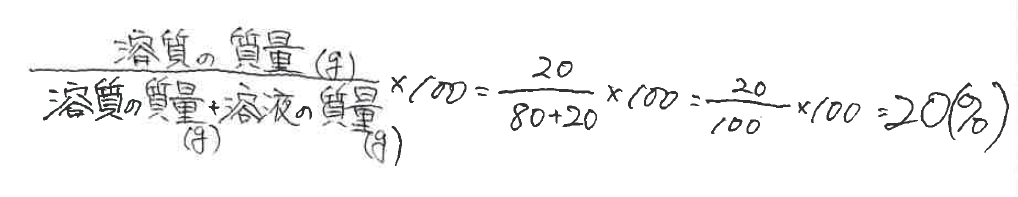



濃度のはなし 中学生向け 質量パーセント濃度について 学習内容解説ブログ



中1理科 濃度 質量パーセント濃度 のポイント Examee
食酢原液の酢酸の質量パーセント濃度を Y 〔%〕とし、食酢原液 1 Lを想定した誘導式は、以下のようになる。 質量パーセント濃度 Y 〔%〕 = × 100 = × 100 = 453 % 実験データの処理(計算例) 溶質の質量溶液に溶けている物質の質量÷溶液の質量×100 で計算し、単位は「 % 」です。質量パーセント濃度(%)= 40(g)÷100(g)×100 = 40% となる。 (2)水に砂糖40 gを溶かしてつくった100gの砂糖水 溶質は砂糖のことであり、質量はg。水溶液は砂糖水のことであり




高校化学基礎 質量パーセント濃度とは 映像授業のtry It トライイット



これで理科マスター 質量パーセント濃度を計算する5つの問題 Qikeru 学びを楽しくわかりやすく
Videos you watch may be added to the TV's watch history and influence TV recommendations To avoid this, cancel and sign in to on your computer An質量/体積(容積)パーセント濃度の求め方 溶質の質量 (g) ÷ 溶液の体積・容積 (ml) × 100 = 質量/体積パーセント濃度 % 体積(容積)ml にしめる、溶質の割合を求める方法です。 質量パーセント濃度は、溶液 100g に占める溶質の割合を求める方法ですが、 質量/体積パーセント濃度の場合は、100ml の体積(容積)にしめる溶質の割合を求める方法です。 注意し モル濃度とは、溶質のモル (mol)/溶液の体積 (L)で表される、入試必出の知識です。 本記事では、溶液、溶媒、溶質の違い、モル濃度と密度、質量パーセント濃度の違い、公式、求め方、関係性について、図と入試頻出の練習問題でわかりやすく解説します




高校化学基礎 質量パーセント濃度とは 映像授業のtry It トライイット




高校化学基礎 硫酸とモル濃度 映像授業のtry It トライイット
は,質量パーセント濃度,若しくは重量パーセント濃度という。溶液も溶質も質量 gの場合であり,w/w% のほかwt% やmass%という表し方もある。単に%の場合は,こ れを指す場合が多い。w/w% = 溶質の質量g 溶液の質量g ×100 で表す。 w/v% は,質量体積パーセント濃度,若しくは質量容積パーセント濃度といい,分子が溶質 の質量一般に,溶液中に含まれる溶質の割合を濃度といい,その表し方には,質量パーセント濃度,モル濃度, 質量モル濃度などがある。濃度に関する出題タイプは,主にⅠ~Ⅶの7つのタイプがある。 例えば,食塩(NaCl)を水(H 2O)に溶かした食塩水を考える。 溶解によって,生じた均一な液体混合物を溶液という 質量パーセント濃度の計算問題集基本編 科学者たちは、質量パーセント濃度という基準をつくり、世界を発展させたことは学びましたよね。 具体的にいえば、 「この溶液が100gあったとき、溶質は何gあるのか? 」 を示す指標です。 質量




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく
質量パーセント濃度 水溶液の質量に対する溶質の質量の比を水溶液の濃度といい、濃度を百分率(%)で表したものを質量パ-セント濃度といいます。 <求め方> (※水溶液=水+溶質) 溶解度と質量パーセント濃度の練習問題 問題1 まずは、一問一答 パーセント濃度は、溶質の質量÷溶液の質量×100です。<数式の挿入> ②で求めた溶質の質量÷①で求めた溶液の質量×100で求められるので、<数式の挿入> 438 ÷ 10 ×100= 365% <数式の挿入> これより、求める質量パーセント濃度は365%となります。質量パーセント濃度 15 % となります。




50g15 0g Descubre Como Resolverlo En Qanda




モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ
方程式の作り方は,最後にできる食塩水の濃度について式を立て, とします. この例では, 12%の食塩水0 (g)には食塩が0×012=24 (g)含まれており,x%の食塩水300gには食塩が300×x÷100=3x (g)含まれているから,これらを混ぜると食塩の合計は 243x (g)になり 質量パーセント濃度の求め方練習問題 水100gに食塩を25g溶かした水溶液の質量パーセント濃度を求めよ。 答えはこちら 水100gと食塩25gを混ぜるのだから、完成した食塩水は となります。 よって、溶液125g、溶質25gとなるから 水340gに塩を60g溶かした(2)質量パーセント濃度を理解し、その表し方、求め方を理解できる。 知識・理解 (3)水溶液から溶質を結晶として取り出す実験を行い、再結晶によって混合物から純粋な物質を取 り出せることを説明できる。 科学的な思考・表現




高校理論化学 溶液の濃度と調製 質量パーセント濃度 密度とモル濃度の単位換算 受験の月
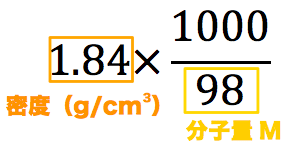



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ



1




中学理科 計算問題 質量パーセント濃度の計算 Youtube




中1 理科 中1 32 質量パーセント濃度 Youtube




1 30g 3100g See How To Solve It At Qanda




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく
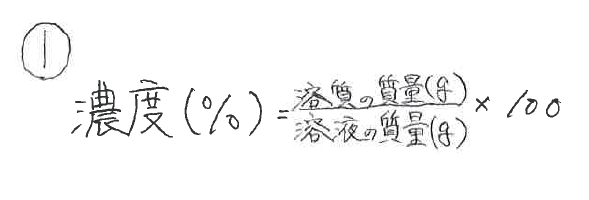



濃度のはなし 中学生向け 質量パーセント濃度について 学習内容解説ブログ




中1理科 質量パーセント濃度 水や塩が増えた時の解き方 Youtube




4 6 溶液の濃度 おのれー Note




質量パーセント濃度




腎臓 計算に必要な基礎知識 濃縮率の求め方 せいぶつ農国




モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ
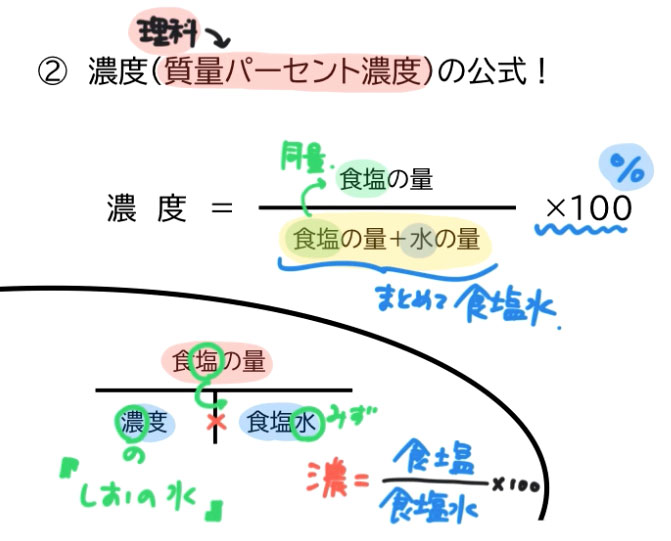



中1理科 数学 食塩水の問題を動画でマスター 公式の覚え方と濃度の計算 マナブレイン



基礎化学3 溶液




質量パーセント濃度の計算問題集 応用編 Menon Network
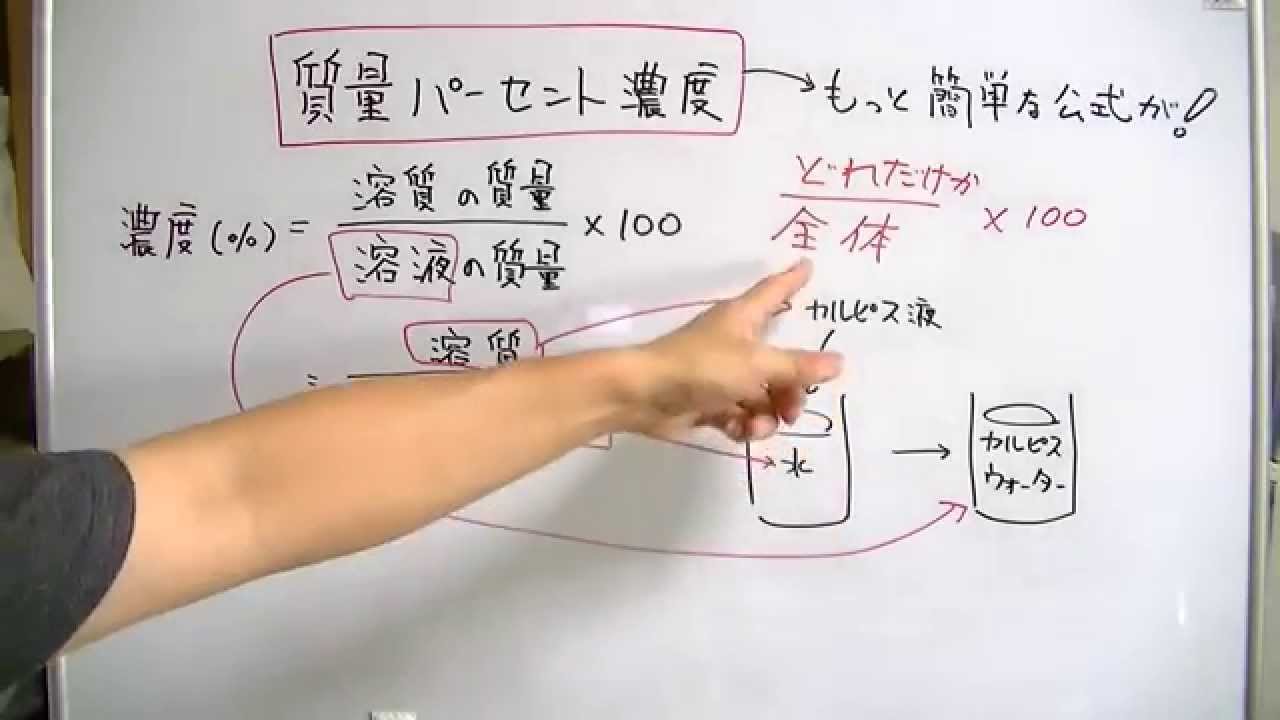



質量パーセント濃度 簡単な公式で覚えよう おときち副塾長 電脳空間学習塾かもん Youtube
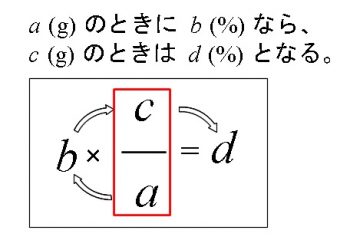



溶液の質量パーセント濃度の求め方と比重を利用した計算問題




モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ



中1理解の 質量パーセント濃度 公式ですが く も わみ Yahoo 知恵袋



3




質量パーセント濃度の求め方 問題を使ってかんたんに解説するぞ 中学数学 理科の学習まとめサイト
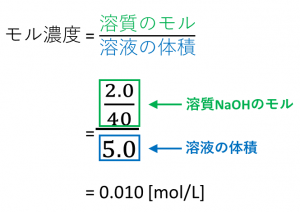



モル濃度と密度 質量パーセント濃度の考え方 Vicolla Magazine



溶質を求める




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




高校化学基礎 濃度の計算 練習編 映像授業のtry It トライイット




濃度 の計算が苦手な方へ 元研究員がわかりやすく解説 Study Z ドラゴン桜と学ぶwebマガジン




濃度について 質量パーセント W W と質量体積パーセント W v 生涯学人 まなびと 楽しいサイエンス 暮らしはサイエンス 子供たち サイエンスを感じて




危険物資格取得のための高校化学no 1 濃度計算 F M サイエンスブログ



化学です 質量パーセント濃度の求め方を教えてください 約分の仕方 が Yahoo 知恵袋
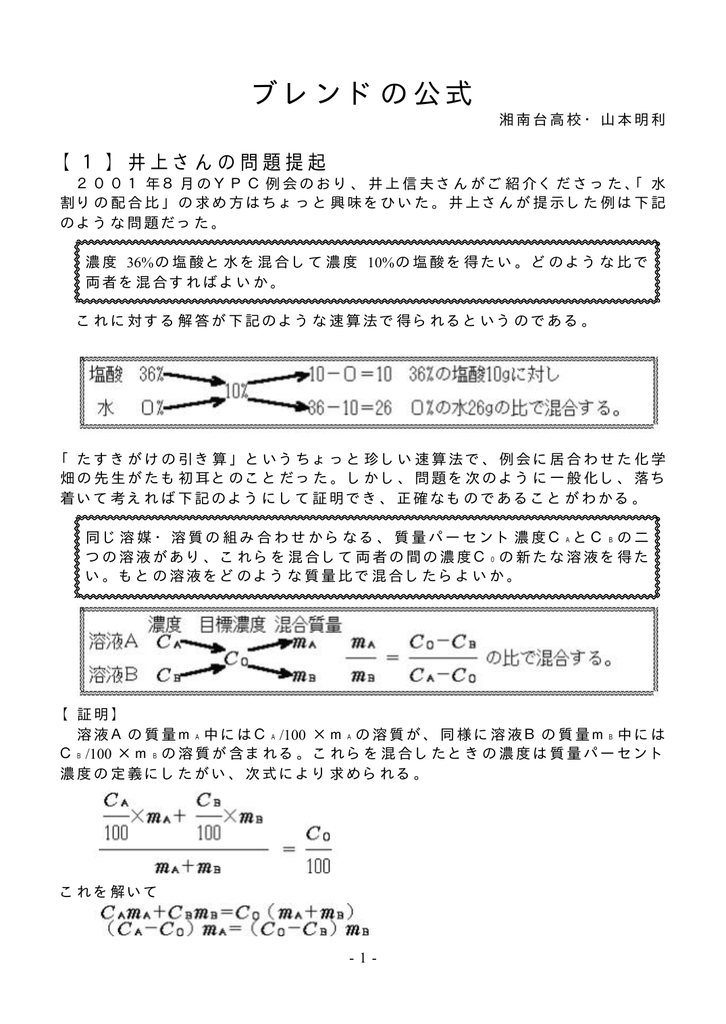



ブレンドの公式 Pdfファイル538kb



質量パーセント濃度の求め方ってこれであってますか 質量パーセ Yahoo 知恵袋



50g15 0g Descubre Como Resolverlo En Qanda



1



基礎化学3 溶液




理科 中1 27 質量パーセント濃度 Youtube




1分でわかる質量パーセント濃度の公式や求め方 基本を登録者数95万人人気講師がわかりやすく解説 Study Z ドラゴン桜と学ぶwebマガジン




濃度のはなし 高校生向け モル濃度と質量モル濃度について 学習内容解説ブログ




モル濃度 Molar Concentration Japaneseclass Jp
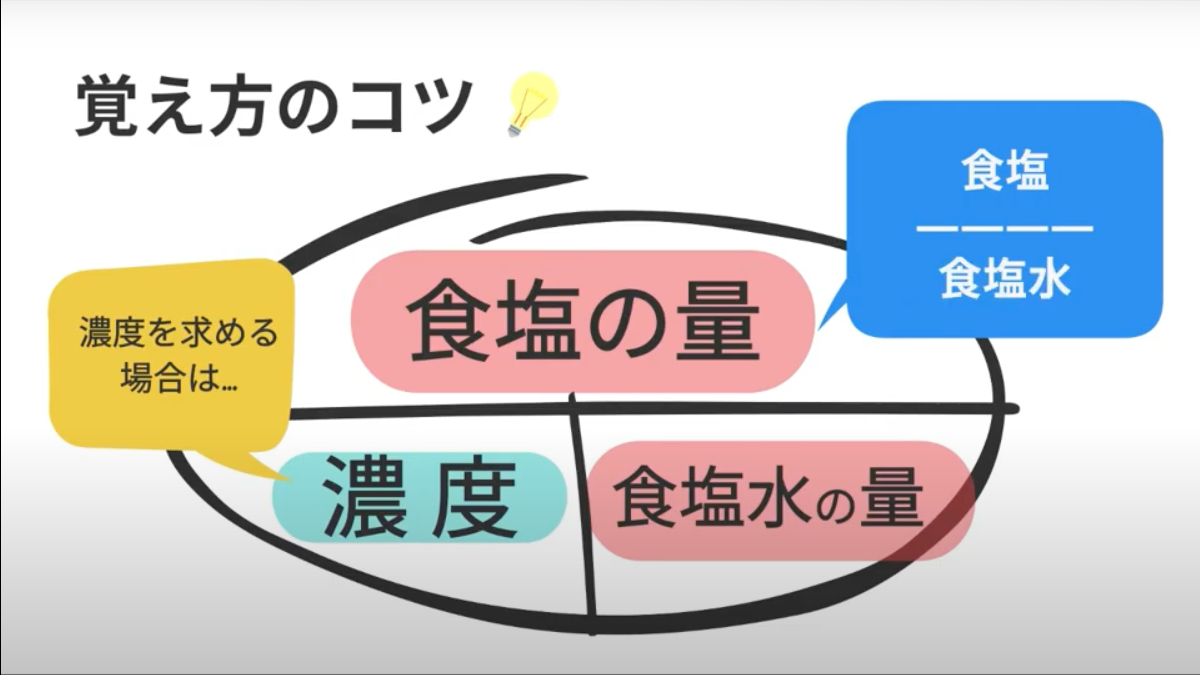



中1理科 数学 食塩水の問題を動画でマスター 公式の覚え方と濃度の計算 マナブレイン




Q21 Ly P Descubre Como Resolverlo En Qanda




化学講座 第12回 濃度と密度 私立 国公立大学医学部に入ろう ドットコム



公式を使う




モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ



濃度の応用




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット
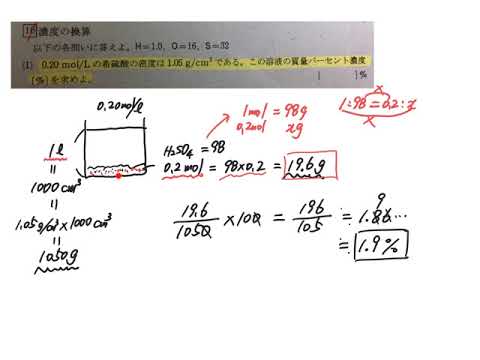



化学 Mol濃度 質量パーセント濃度 Youtube



Mol濃度 質量パーセント濃度 質量モル濃度の相互変換の仕方のコツ




中1理科 水溶液 濃度の計算が10分で理解できる たけのこ塾 勉強が苦手な中学生のやる気をのばす




2 質量パーセント濃度の求め方がわかりません Clear




高校理論化学 食酢中の酢酸のモル濃度と質量パーセント濃度 受験の月



質量パーセント濃度



モル濃度と密度 質量パーセント濃度の考え方 Vicolla Magazine




1分でわかる質量パーセント濃度の公式や求め方 基本を登録者数95万人人気講師がわかりやすく解説 ページ 4 4 Study Z ドラゴン桜と学ぶwebマガジン




高校化学基礎 濃度の計算 練習編 映像授業のtry It トライイット
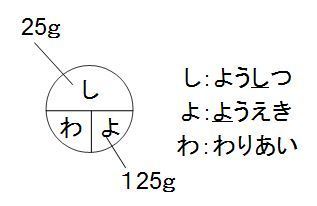



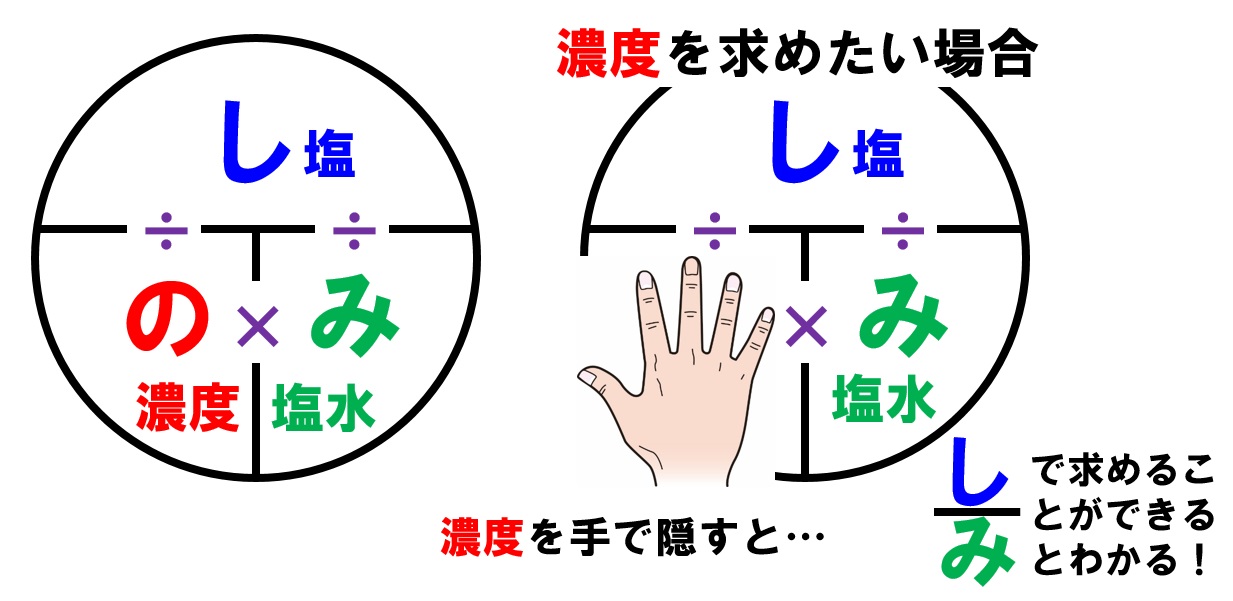
しわよ で覚える質量パーセント濃度 中学テスト 入試対策ノート




برچسب 質量パーセント濃度 در توییتر




理科の パーセント濃度 の計算問題 教えて欲しいです 出来なくて Clear
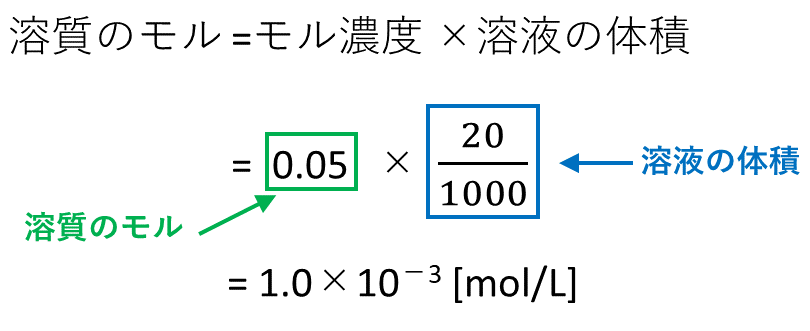



5分でわかる モル濃度と密度 質量パーセント濃度の考え方を図と練習問題付きで徹底解説 サイエンスストック 高校化学をアニメーションで理解する




濃度が10 の食塩水250gに水を加えて濃度が8 の食塩水をつくりたいときに必要な水 Clear




質量パーセント濃度の求め方とモル濃度の違い
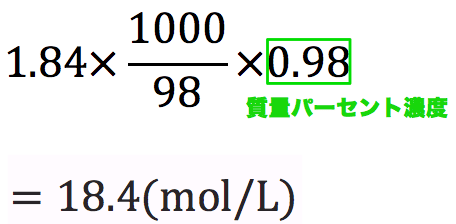



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ




質量パーセント濃度 密度で求められるのは質量ですか Clear




エレガント質量 パーセント 濃度 最高のぬりえ




4 6 溶液の濃度 おのれー Note




質量パーセント濃度の計算問題集 基本編 Menon Network




原子百分率の計算方法 備忘録 T Nakaの阿房ブログ




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット



濃度のはなし 中学生向け 質量パーセント濃度について 学習内容解説ブログ




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




これで理科マスター 質量パーセント濃度を計算する5つの問題 Qikeru 学びを楽しくわかりやすく




高校生物基礎 腎臓のイヌリン濃縮率や原尿量などの計算問題の解き方 高校生物の学び舎




Wt 重量パーセント Mass 質量パーセント とは 計算方法は 演習問題



中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu




これで理科マスター 質量パーセント濃度を計算する5つの問題 Qikeru 学びを楽しくわかりやすく




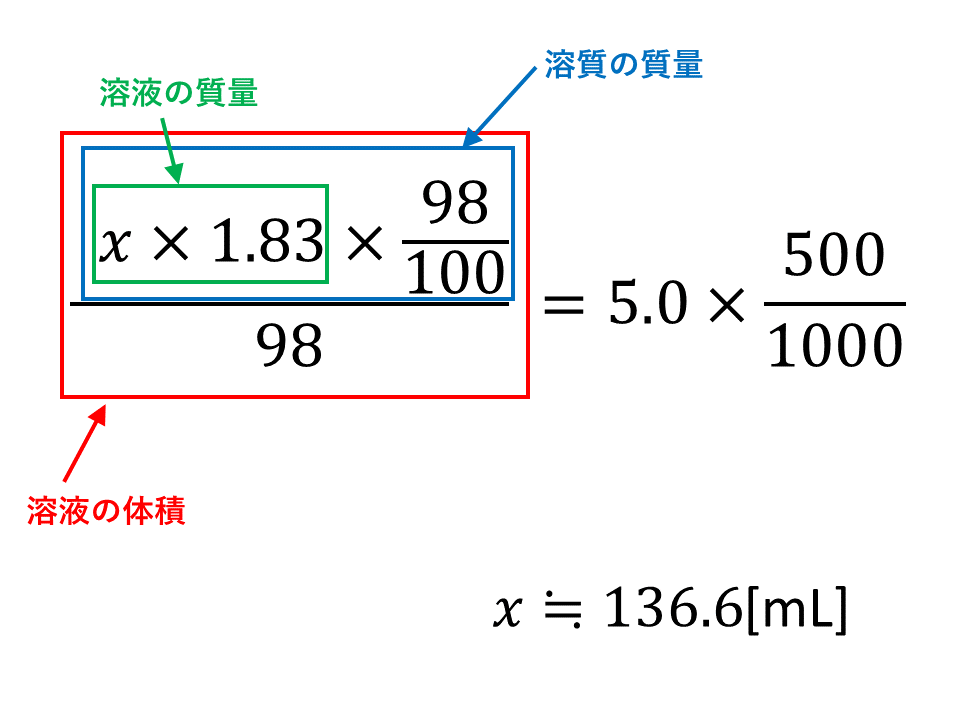
至急 質量パーセント濃度が98 の濃硫酸の密度は1 8g Cm3である この 高校 教えて Goo




4 質量パーセント濃度の求め方を教えてください Clear




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




4 6 溶液の濃度 おのれー Note



モル濃度 質量パーセント濃度 質量モル濃度 濃度計算のコツも解説 受験メモ
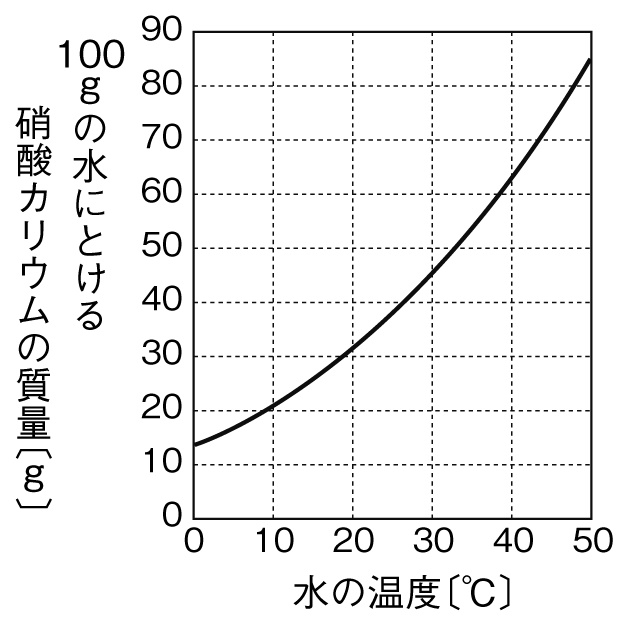



定期テスト対策問題 質量パーセント濃度の計算演習問題 Examee




Mol濃度 質量パーセント濃度 質量モル濃度の相互変換の仕方のコツ



N8jvc6g Net Archives 2440
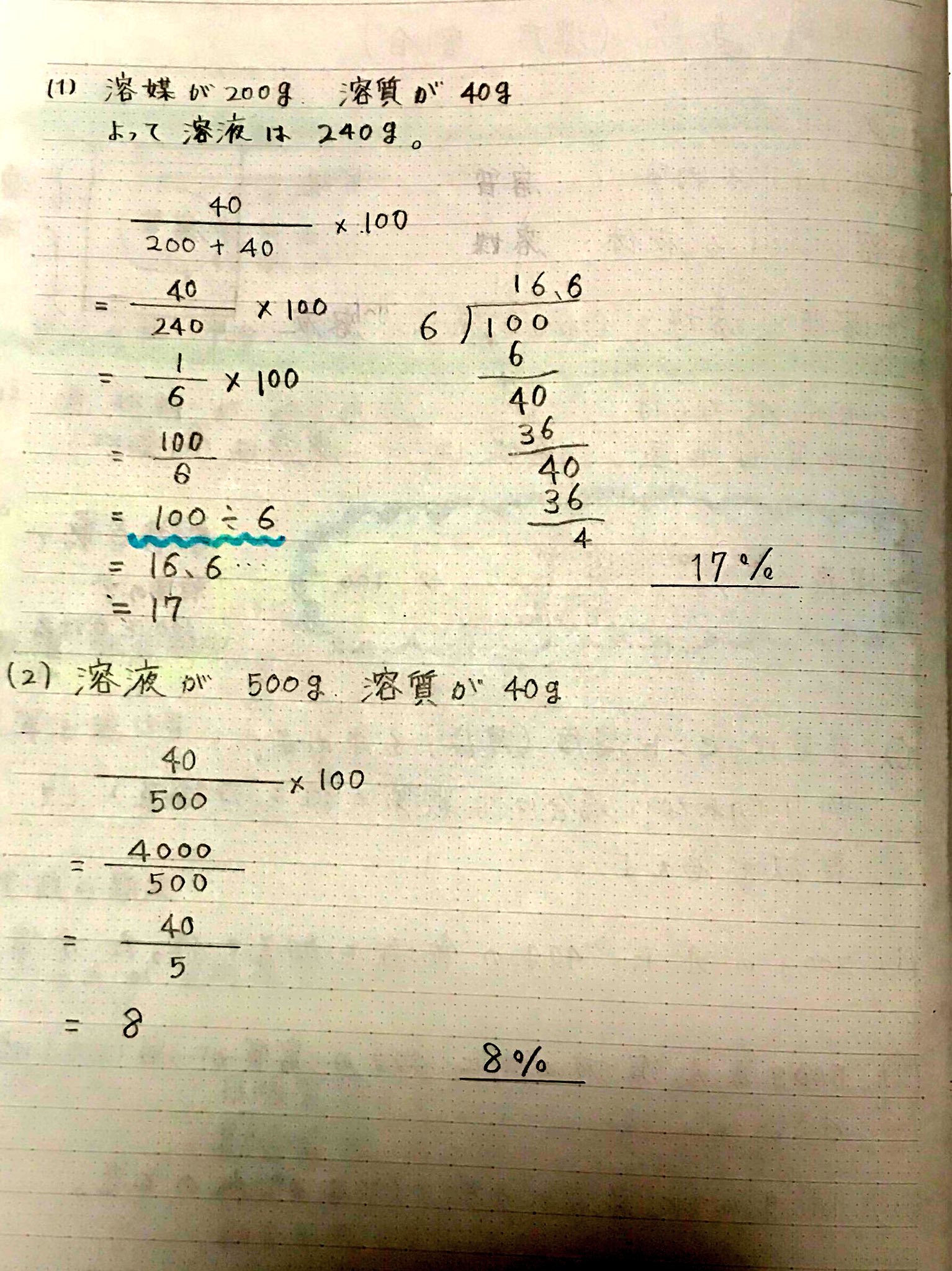



Akiya Su 理科 質量パーセント濃度 溶質 溶媒 溶液と公式を覚えること 計算は難しくないが 割り算の筆算で小数点の位置がわからない人は先生に聞こう 中学理科 質量パーセント濃度
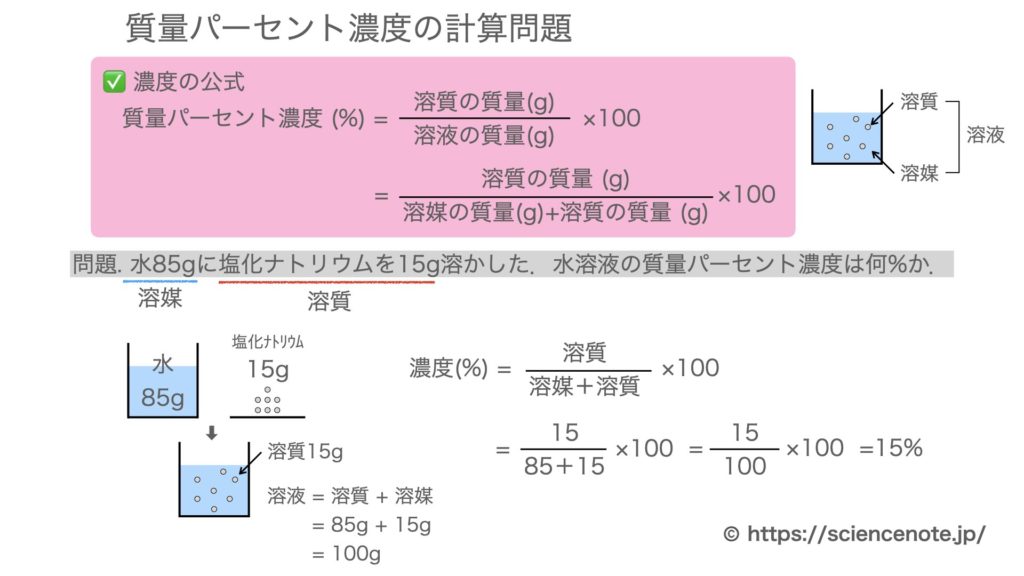



水溶液と質量パーセント濃度の計算問題 Hiromaru Note




質量パーセント濃度に関する問題です 0 4がどこから出てきたのかわかりません Clear



Thinkstock Images




溶液の濃度 無料で使える中学学習プリント



1
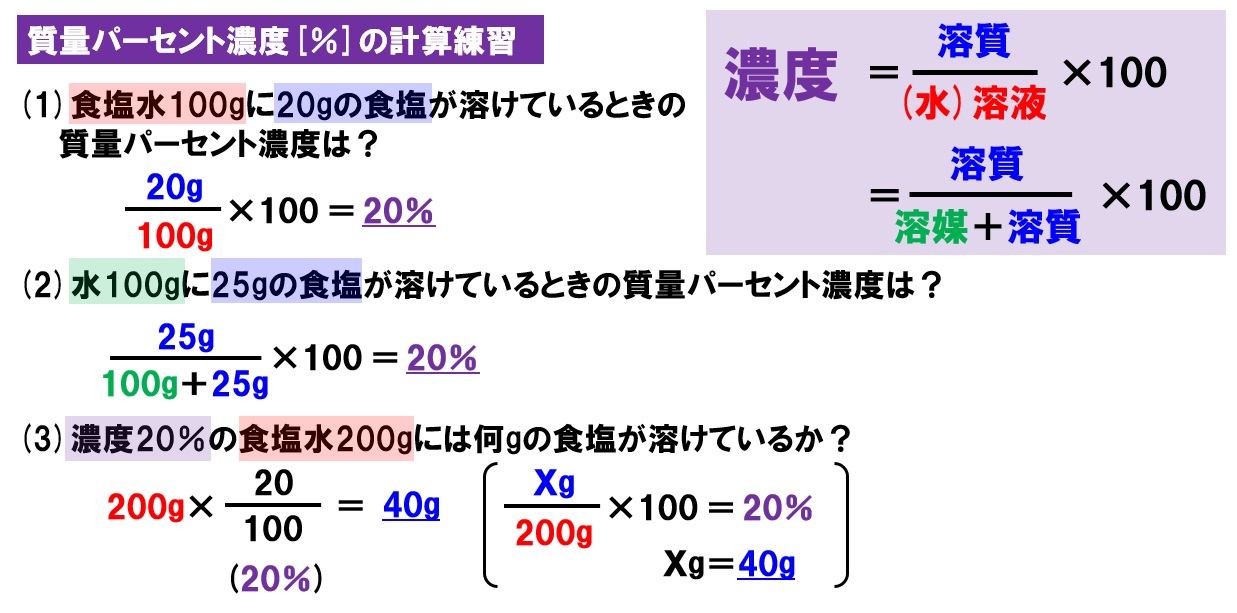



中1理科 水溶液と濃度 水溶液の性質と濃度計算 Pikuu


